בשנים האחרונות עולם המדע חוקר בקפידה את מגמות העבר של התפרצויות נגיפיות, שכמה מהן החלו בעטלפים. בזכות מערכת חיסון ייחודית, עטלפים מסוגלים לארח נגיפים רבים מבלי לחלות בעצמם. לעיתים נוצרים זנים חדשים מתוך המגוון הגנטי העצום של הנגיפים שהעטלפים נושאים, זנים שיכולים לרכוש תכונות המאפשרות להם להדביק גם בני אדם, ולגרום בהם למחלה. מחקר חדש שנערך בסין התמקד בנגיף HKU5-CoV-2 המציג יכולת מרתקת להתחבר לחלבון ACE2 האנושי – אותו קולטן מפורסם שמנצל גם נגיף SARS‑CoV‑2, הגורם למחלת ה‑Covid‑19.
עטלפון הבית היפני (Pipistrellus abramus) הוא עטלף הנפוץ באזורים עירוניים וכפריים במזרח אסיה. הוא ניחן במידות גוף קטנות וביכולת להסתגל למגוון סביבות. עטלף זה הוא מקור טבעי עשיר לנגיפים, שכן הוא נושא קשת רחבה של נגיפים מבלי לסבול מתסמינים חריפים, מה שמצביע על מערכת חיסון מיוחדת ועמידה (דומה לזו של מיני עטלפים אחרים) [1, 2].

עטלפון הבית היפני. איור: DataBase Center for Life Science (DBCLS)
כמו ביונקים אחרים, גם בעטלף זה נמצא החלבון Angiotensin-Converting Enzyme 2 (ובקיצור ACE2). חלבון זה נמצא על פני תאי רקמות רבות בגוף האדם, בין היתר במערכת הנשימה, בלב, בכליות ובמעיים. תפקידו המרכזי הוא ויסות מערכת הרנין-אנגיוטנסין, אשר אחראית על ויסות לחץ הדם והמאזן החשמלי של התאים. ACE2 משמש כקולטן וכנקודת הכניסה לתאי הגוף של נגיפי קורונה שונים, וביניהם SARS‑CoV‑2. הנגיפים מזהים אזורים ספציפיים בחלבון ומתחברים אליהם, מה שמאפשר להם לחדור לתאים, שם הם משוכפלים. כמו כן, חלבון הזיזים (SPIKE - הבולט ממעטפת הנגיף) המפורסם של הנגיף מתפקד כמפתח כניסה המתקשר ישירות עם חלבון ה-ACE2, וכך מאפשר את חדירת הנגיף לתא. אם שמו של חלבון זה נשמע לכם מוכר, אינכם טועים! זהו החלבון שיוצר בחיסוני ה-mRNA המפורסמים נגד ה-SARS-CoV-2.
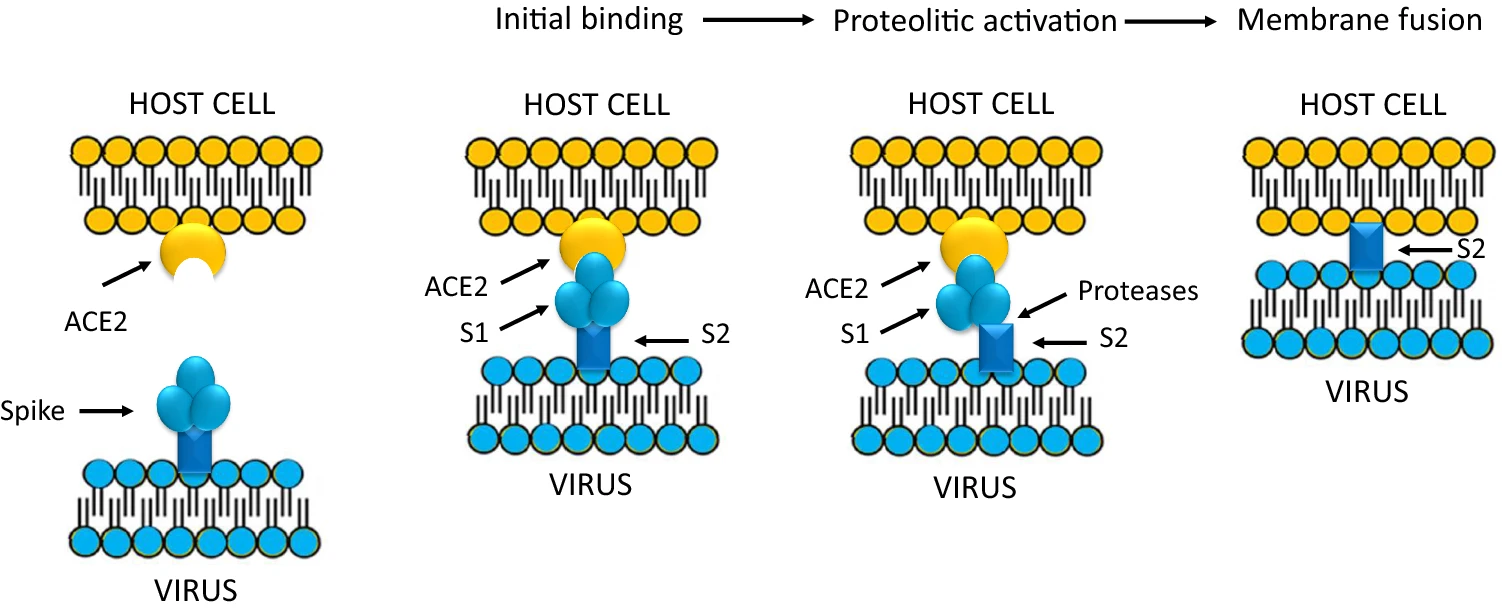
איך חלבון הזיזים של נגיפי קורונה עוזר להם לזהות את תא המטרה. מקור: Rossi et al. Infection 2020
המעבר בין מיני פונדקאים הוא תהליך מורכב עבור הנגיף, ומעורבות בו התאמות ברמה המולקולרית. נגיף HKU5-CoV, שזוהה כבר בשנת 2006, היה מוגבל בעבר לעטלפים בלבד – הוא התחבר אך ורק לחלבון ה-ACE2 של העטלפים והתרבה רק בהם, בלי להשפיע על בני אדם. אולם מחקר חדש שערך צוות סיני בהובלת פרופ' ג'ינג צ'ן (Jing Chen) ממכון ווהאן לווירולוגיה (כן, אותו מכון מפורסם) וד"ר זנג‑לי שי (Zheng-Li Shi) מהמעבדה הלאומית בגואנגג'ואו, חשף כי זן חדש של הנגיף, HKU5‑CoV‑2, עבר סדרת מוטציות משמעותיות בחלבון ה‑SPIKE שלו, ובמיוחד באזור המתקשר לקולטן, שבעקבותיהן הוא מצליח להיקשר גם לתאים אנושיים בתרבית. באמצעות כלים מתקדמים, החוקרים הצליחו לקבל תמונה ברורה של המנגנון המולקולרי המאפשר לנגיף להתחבר בצורה יעילה ל-ACE2 האנושי. המחקר פורסם במגזין היוקרתי Cell.
נתונים שפורסמו במחקר מספקים הצצה מעמיקה למבנה הקשר בין הנגיף ל-ACE2. בעזרת מיקרוסקופיית אלקטרונים (Cryo‑EM) התגלה כי הקישור בין החלבונים נעשה באמצעות שני אזורים עיקריים, שבהם מתרחשות אינטראקציות חשמליות (מטענים מנוגדים) והידרופוביות (דחיית מים). אינטראקציות אלו מחזקות את הקשר בין חלבון ה-SPIKE ל-ACE2. עוצמת הקישור נמדדה בשיטות כימות מתקדמות, והתקבלו ערכים המעידים על זיקה משמעותית. יש בכך הסבר ליכולתו של הנגיף ליצור חיבור חזק עם תאים אנושיים בתנאי מעבדה.
המחקר גם עוקב אחר שלבי ההשתנות של החלבון הנגיפי במעבר מהעטלף לתאי אדם, ומציג סדרת תרשימים המבוססים על השוואות "טביעת האצבע" מול חלבון ה-ACE2 של נגיפים אחרים. התרשימים מראים כי למרות שחלק מהאזורים שבהם הנגיף המדובר (HKU5‑CoV‑2) נצמד ל-ACE2 דומים לאלו של נגיפים אחרים, קיימים הבדלים מובהקים המעידים על מסלול אבולוציוני עצמאי.
מעבר של נגיפים מעטלפים לבני אדם אינו תופעה חדשה. בעבר, נגיף SARS‑CoV‑1 שגרם למחלת הסארס הגיע אלינו דרך "חיות ביניים" כמו זבד הדקל המסכתי (Paguma larvata), ואילו נגיף MERS‑CoV שגרם למחלת המרס עבר אלינו דרך גמלים. עדיין לא ידוע אם HKU5‑CoV‑2 יעבור לאדם ישירות או שתידרש חיית ביניים, אך יכולתו של הנגיף להתחבר ל-ACE2 האנושי במעבדה מעוררת חשש לגבי הפוטנציאל שלו להתפשט בעתיד.

זבד הדקל המסכתי (masked palm civets - Paguma larvata). מקור: Wikimedia Commons
ההבנה המעמיקה של ההתאמות המולקולריות המאפשרות לנגיפים לעבור ממארח למארח היא קריטית לפיתוח מערכות אבחון מהירות, תרופות וחיסונים, וכן להיערכות מוקדמת למניעת מגפות עתידיות. המחקר שעליו אנו מדווחים כאן מהווה תמרור אזהרה ומדגיש את הצורך במעקב צמוד ובמחקר נוסף בתחום, מכיוון שכל מוטציה קטנה במבנה ה-SPIKE יכולה להשפיע על יכולתו של הנגיף לחדור לתאי הגוף ולהפיץ את עצמו. על פי המחקרים הנוכחיים, נראה כי למרות שהנגיף מסוגל להתחבר ל‑ACE2 האנושי ולחדור לתאי אדם בתנאי מעבדה, הוא אינו מציג את המאפיינים הקליניים או את יעילות הקישור הגבוהה שנצפים אצל נגיפים כמו SARS‑CoV‑2. כלומר, במצבו הנוכחי, הסיכוי שהוא יהיה פתוגן (מחולל מחלה) חזק בבני אדם אינו גבוה במיוחד. עם זאת, חשוב להדגיש שמצב זה עלול להשתנות; שינוי קטן או מוטציה עתידית עלולים לשנות את יכולת ההדבקה ואת הפתוגניות של הנגיף, לכן יש חשיבות למחקר ומעקב מתמשכים.
סיפורו של HKU5‑CoV‑2 הוא תזכורת חשובה לכך שהטבע מלא בהפתעות. ההתאמות האבולוציוניות העדינות של נגיפים, השילוב בין המנגנונים המולקולריים והתהליכים הגנטיים המורכבים, כל אלו מלמדים אותנו עד כמה העולם המיקרוסקופי יכול להשפיע על בריאות הציבור. אומנם עד כה לא תועדו מקרים טבעיים של הדבקה בבני אדם, אך המחקר מציג מנגנון מולקולרי מעניין ומעלה שאלות מהותיות, לכן הקהילה המדעית וארגוני הבריאות נדרשים להמשיך לעקוב, לחקור ולהיערך בהתאם.
מסע מדעי זה, המבוסס על מחקרים יסודיים ונעזר בכלים טכנולוגיים מתקדמים, אינו רק סיפור של גילוי, אלא גם של אתגר עתידי בהכנה של המין האנושי להתמודדות עם פתוגנים שעוברים מבעלי חיים לבני אדם, דבר שכבר קרה פעמים רבות בעבר. החוקרים קוראים להמשך מחקר כדי להגיע להבנה מעמיקה של האינטראקציות בין עולמות שונים, במיוחד בין עולמם של העטלפים לבין בני האדם. אנו נמשיך לעקוב ולדווח לכם, כמובן.
עריכה: סמדר רבן
מקורות והרחבות
[1] על דלקות, נגיפים ועטלפים - שקד אשכנזי - מדע גדול, בקטנה - 2018
[2] המעופפים העמידים - יומירן ניסן - מדע גדול, בקטנה - 2025
[3] SARS - מחלה חדשה ומאיימת - דרור בר-ניר - 2006
[4] נגיף קורונה (MERS-CoV) חדש וקטלני צץ בחצי האי ערב - דרור בר-ניר - 2013
[5] הנגיף הטוען לכתר - דרור בר-ניר, מדע גדול בקטנה - 2020
[6] המאמר המקורי - בכתב העת Cell - מרץ 2025