ניסוי קליני ראשון מציג רפואה מותאמת אישית לטיפול בגידולים סרטניים. חוקרים הינדסו תאי מערכת חיסון לזהות חלבונים ייחודים לגידול של כל חולה. הדבר התאפשר בעזרת שילוב שתי טכנולוגיות מבטיחות מעולם הביוטק.
"תאי T הורגים" (נקראים גם תאי T ציטוטוקסיים), הם תאי דם לבנים השייכים למערכת החיסון שלנו. הם מסוגלים לזהות תאים בגופנו שהודבקו בנגיפים, חיידקים ואפילו תאים סרטניים. הזיהוי מתאפשר בעזרת מנגנון שקיים בכל תאי הגוף שלנו, שתפקידו להציג לתאי מערכת החיסון חלקים קטנים מחלבונים שנמצאים בתוך התא. לתאי ה-T יש קולטנים המסוגלים לזהות חלבונים "זרים", כך שאם תא הודבק בנגיף, למשל, הוא יציג על פניו חלבונים נגיפיים, מה שבתורו יאפשר לתאי ה-T להבין שמשהו אינו תקין באותו התא ולחסל אותו [1].
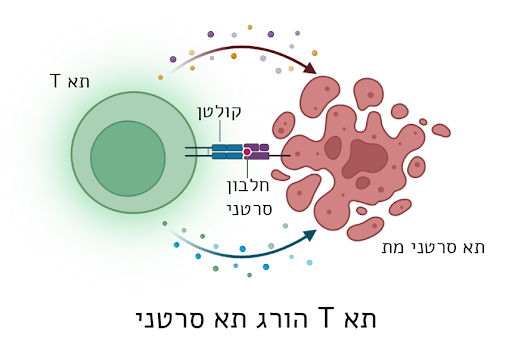
קרדיט: נוצר באמצעות BioRender.com
מה לגבי תאים סרטניים? רוב החלבונים המיוצרים על ידי תאים סרטניים הם חלבונים "רגילים", שזהים לשאר חלבוני הגוף שלנו. עם זאת, מכיוון שבתאים אלו נוצרות מוטציות ברצף ה-DNA, הדבר יכול לגרום גם להיווצרות של חלבונים מוטנטיים, שיהיו ייחודיים לתאי סרטן אלו ביחס לשאר תאי הגוף. מכיוון שחלבונים אלו שונים מהחלבונים הרגילים של הגוף, תאי ה-T יכולים לזהות אותם ולחסל את התאים הסרטניים.
על מנת לחסל תאי סרטן ביעילות ומהירות נדרשת כמות גדולה של תאי T שמוכוונים נגד הגידול ומזהים היטב את החלבונים ה"סרטניים". הבעיה היא שבפועל, המנגנון הטבעי לחיסול הסרטן על ידי תאי T איננו מאוד יעיל. מה שמגדיל את הקושי אף יותר בהתמודדות עם גידולים סרטניים הוא העובדה שבמקרים רבים הם מצליחים לחסום את התגובה החיסונית, למשל על ידי הפרשת מולקולות שהורגות או מעכבות את תאי T המיועדים להרוג אותם, ועל ידי רתימת תאי חיסון אחרים שדווקא מסייעים להם לגדול [2-4].
כאן נכנסת לתמונה טכנולוגיית Chimeric Antigen Receptor T cells, או בקיצור: CAR-T. בטכנולוגיית CAR-T מהנדסים תאי T כך שיילחמו טוב יותר נגד סרטן [5-6]. את תאי ה-T מבודדים מחולה הסרטן עצמו, מרבים אותם מחוץ לגופו, ואז מחזירים אליו "צבא" של תאי T מהונדסים, הכוללים קולטן שמסוגל לזהות תאים סרטניים, על מנת שיצודו ויחסלו אותם ביעילות רבה יותר; הקולטן המהונדס מפעיל את תאי ה-T חזק יותר מהקולטן הטבעי, וכן מייצרים תאים רבים כאלה, כך שהם מנצחים גם במספרים.
נכון לעכשיו פותחו כמה טיפולי CAR-T אשר מאושרים לשימוש. טיפולים אלו נפוצים בסוגים שונים של סרטני דם אך לא בגידולים מוצקים. מדוע? גם סרטני דם וגם גידולים מוצקים מאופיינים בתאים שמתחלקים ללא בקרה, אך בגידול מוצק מדובר בגוש (או כמה גושים) של תאים שמתפתח בצורה שאינה אחידה בכל נפחו, וכך מגוון החלבונים הקיים בתאי הגידול השונים, באותו חולה ובגידולים של חולים שונים, גדול. לעומת זאת, בסרטני דם ישנו דמיון רב בין התאים, המבטאים חלבונים הדומים אחד לשני ובין חולה אחד לאחר. כך מתאפשר שימוש באותם קולטנים אצל מטופלים שונים בעלי אותו סוג סרטן דם, דבר שאינו אפשרי בגידולים מוצקים, שבהם נדרש טיפול מותאם אישית לכל חולה.
עד כה, תהליך הנדסת התאים ב-CAR-T התבצע באמצעות הדבקת התאים בווירוס, והצריך פיתוח ארוך שנים של כל מוצר לפני שהוא מגיע לחולים. טכנולוגיית עריכת הגנים CRISPR, שעליה כתבנו רבות בעבר [7], יכולה לאפשר הנדסה מהירה של תאי T המתאימים לחלבונים הספציפיים של כל חולה סרטן.
במחקר שהתפרסם בחודש שעבר [8-9] בכתב העת Nature, החוקרים השתמשו ב-CRISPR על מנת להנדס תאי T מותאמים אישית לחולי סרטן עם גידולים מוצקים שלא הגיבו לטיפולים אחרים. תחילה ריצפו החוקרים DNA מהדם ומהגידולים של החולים, והשוו את רצף ה-DNA האישי של כל חולה לזה של הגידול שלו, על מנת למצוא חלבונים בעלי מוטציות בתאי הסרטן שתאי ה-T יוכלו לזהות כגורם זר. בשלב הבא הם סרקו קולטנים של תאי T שבודדו מהחולים על מנת למצוא את אלו שמזהים הכי טוב את אותם חלבונים "זרים". באמצעות טכנולוגיית CRISPR/CAS9 הם הכניסו לתאי ה-T שבודדו מגוף החולה "הוראות" (גנים) לייצור הקולטנים המוצלחים. לכל חולה ייצרו "צבא" של עד שלושה סוגי תאי T המותאמים לתקוף את הגידול שלו, והחזירו אותם לגוף החולה.
הטיפול הראה הצלחה מוגבלת — מתוך 16 חולים שהשתתפו במחקר חמישה הראו מחלה יציבה, שבה הגידול לא המשיך להתפתח. זהו אמנם מספר קטן אך צריך לזכור - מדובר בכ-30% מהמטופלים, ששאר הטיפולים הקיימים לא עזרו לעצור את מחלתם. החוקרים, שהחזירו לגוף החולים מספר מוגבל של תאי T מהונדסים מטעמי בטיחות, בטוחים כי שימוש בצבא נרחב יותר יביא לתוצאות מרשימות בהרבה.
המהירות והיכולת לערוך גנים באופן כמעט בלתי מוגבל באמצעות CRISPR הן יתרון אדיר — זהו איננו עוד "מוצר מדף", בדומה לטיפולי ה-CAR-T הנמצאים כרגע בשוק, אלא פוטנציאל לטיפול מותאם אישית לחולה שיכול להגיע אליו לפני שיהיה מאוחר מדי. החוקרים מקווים שבעתיד — בעזרת התקפה מאסיבית יותר של גידולים באמצעות תאי T מהונדסי CRISPR המותאמים לגידול של החולה, שיוכלו בזכות מספרם הרב לחמוק מהדיכוי החיסוני שהגידול משרה — יושגו תוצאות דרמטיות וחיי חולים רבים יותר ינצלו.
עריכה: ינון קחטן
מקורות והרחבות:
- כתבה על איך תאי T פועלים
- מאמר סקירה על מנגנוני ההתחמקות של גידולים ממערכת החיסון
- השתלת צואה משפרת את התגובה לאימונותרפיה במלנומה
- שיטה להפיכת תאי מערכת החיסון מתומכי גידול לנוגדי גידול
- פוסט על הנדסה גנטית של תאי T נגד סרטן
- פרס ישראל זליג אשחר על פיתוח CAR-T
- פוסט על CRISPR/Cas9 לכבוד פרס נובל לשנת 2020
- המאמר המקורי
- דיווח חדשותי בכתב העת Nature אודות המחקר