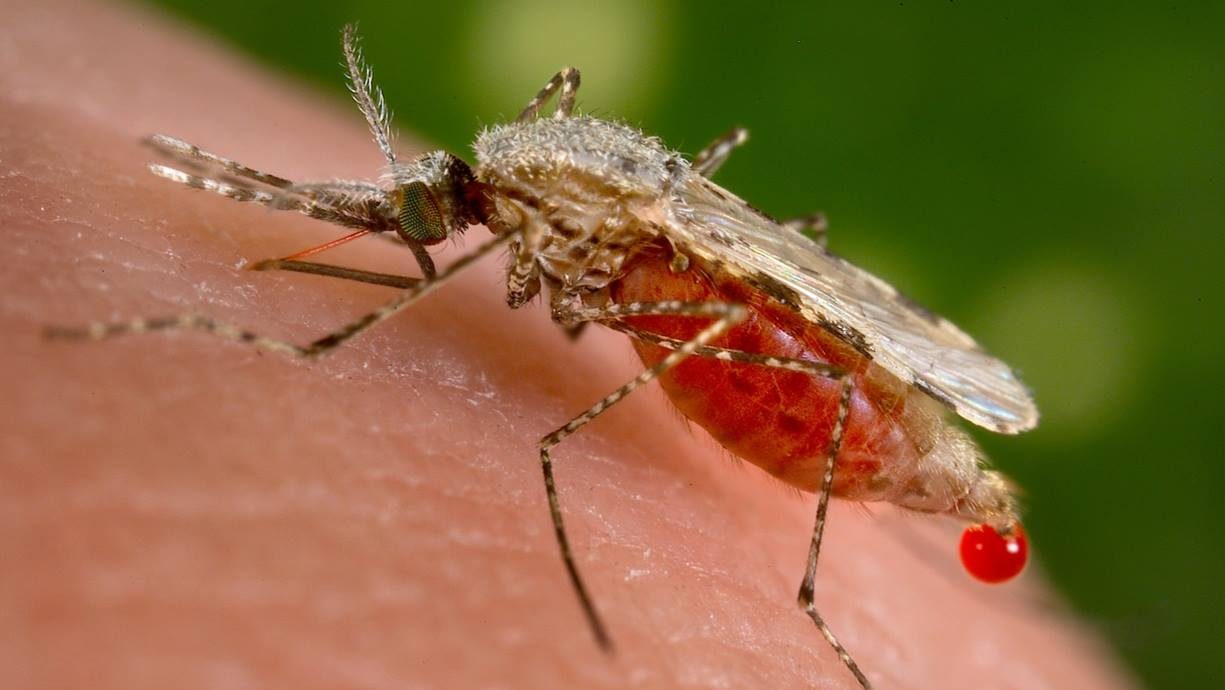
בקטנה: מחקר בריטי פיתח שיטה גנטית לעיקור המוני של יתושות במטרה לבלום את ההתפשטות של מחלת המלריה.
מלריה היא מחלה קשה שגורמת למותם של מאות אלפי בני אדם בכל שנה, רובם ילדים ונשים הרות באפריקה. על פי הערכות ארגון הבריאות העולמי [1], למעלה מ-200 מליון בני אדם חלו במלריה בשנת 2015, מתוכם מתו כ-429,000 (כ-50 נפטרים בכל דקה!). המחלה נגרמת על ידי טפיל הפלסמודיום שמועבר מאדם לאדם באמצעות עקיצה של יתושת אנופלס.
הרוב המוחלט של מקרי המלריה הם במדינות עולם שלישי ללא נגישות לטיפול רפואי, ולכן האסטרטגיה המרכזית במאבק העולמי במחלה היא ניסיון למנוע הדבקה, בעיקר באמצעות צמצום החשיפה ליתושות האנופלס על ידי מיגון אישי, חומרי הדברה, ייבוש מקורות מים עומדים וכד'.
כיצד ניתן למגר את ההדבקה במחלה? קבוצת חוקרים מה-Imperial College בלונדון פרסמה בסוף 2015 מחקר שמציע פיתרון "נקי" וחדשני – עיקור גנטי של יתושות, ושחרור של אותן יתושות עקרות בכדי שיפיצו עקרות בקרב הצאצאים שלהן ויבלמו את התרבותם.
רגע, מה? הפצת עקרות לצאצאים? איך יתושה עקרה יכולה להעמיד צאצאים? כאן נמצא הרעיון היצירתי הראשון של קבוצת המחקר. החוקרים איתרו גן שמעורב בפוריות של יתושות, ופגעו בו כך שיתושות הומוזיגוטיות (בעלות שני עותקים פגועים של הגן) הן עקרות, אבל יתושות הטרוזיגוטיות (עותק אחד תקין ועותק אחד פגוע) מסוגלת להתרבות ולהעביר לצאצאים את אחד משני העותקים – או הפגוע או התקין.
החוקרים השתמשו בטכנולוגיית הקריספר (CRISPR/Cas9), טכנולוגיה חדישה שצברה תאוצה רבה בשנים האחרונות (ראו פוסטים קודמים שלנו בנושא להרחבה), אשר אפשרה להם לפגוע באופן ממוקד בגן הרצוי – הגן שמעורב בפוריות היתושות. זה רעיון יפה מאוד, אבל הוא לא מספיק, שכן הלחץ האבולוציוני פועל בעד העותק התקין ולא העותק הפגום (כלומר, תוך מספר דורות, תכונת העקרות נעלמת מהאוכלוסייה). מסיבה זו, יש למצוא דרך להתגבר על אותו לחץ, ולגרום לכך שדווקא העותק הפגוע שגורם לעקרות יופץ באוכלוסייה. כיצד עושים זאת? המפתח הוא תופעה גנטית שנקראת gene drive, בה גן מסוים משתלט על התורשה הרגילה ו"דוחף את עצמו" אל הצאצאים [3]. בכדי לעשות זאת, קבוצת המחקר יצרה מערכת גנטית מתוחכמת במיוחד – הם לא הסתפקו בפגיעה בגן הפוריות, אלא החליפו אותו ב-Cas9 שיזהה את אותו הגן בכרומוזום השני, ויערוך גם אותו. במילים אחרות, הם יצרו מערכת שבה יתושה הטרוזיגוטית הופכת להומוזיגוטית ויש לה שני עותקים של הגן הפגום.
התחכום לא נגמר כאן – המערכת מתוכננת כך שהיתושה מתפתחת באופן נורמלי, מייצרת ביציות, ורק כאשר הן בשלות הן הופכות מהטרוזיגוטיות להומוזיגוטיות. כלומר, היתושה מתרבה באופן תקין, אבל צאצאיה יקבלו את המטען הגנטי לעקרות באופן כמעט ודאי. יתושים זכרים יכולים להיות בעלי גן פגוע והם יכולים להוריש אותו לצאצאיהם, אבל הם עצמם אינם מושפעים מכך. אם כך, כתוצאה מהטיפול אנחנו מקבלים שלוש אוכלוסיות אפשרויות של יתושות: א. יתושות שיש להן שני עותקים תקינים והן פוריות. ב. יתושות שנולדו הומוזיגוטיות והן עקרות. ג. יתושות הטרוזוגוטיות שהן פוריות בעצמן אבל כמעט בטוח שיעבירו לצאצאיהן גן פגוע. ככל שיהיו יותר יתושות (ויתושים) מהאוכלוסייה השלישית, כך יגדל הסיכוי לקבל יותר יתושות הומוזיגוטיות עקרות, ואוכלוסיית היתושים תקטן בניגוד ללחצים האבולוציוניים. אם יהיו פחות יתושים, יהיה גם פחות מי שיעקוץ ויפיץ את טפיל הפלסמודיום שגורם למלריה.
לסיכום – הפתרון שמציעים החוקרים איננו מושלם, ובעצמם מצביעים במאמר על כמה נקודות תורפה. אולם, הוא מדגים חשיבה מאוד יצירתית, ובהחלט יש מקום לשלב את האסטרטגיה הזו עם אסטרטגיות נוספות למיגור מחלת המלריה.